Bạn đang gặp khó khăn khi học đến số mol, nồng độ mol, nồng độ phần trăm trong môn Hóa Học trung học cơ sở thì bài viết bên dưới đây của chúng tôi sẽ giúp các bạn ôn tậm lại các công thức tính số mol, công thức tính nồng độ mol và công thức tính nồng độ phần trăm đầy đủ, chi tiết.
Công thức tính số mol
Số mol được kí hiệu là chữ n và để tính được số mol các bạn có thể áp dụng các công thức tính bên dưới đây chúng tôi chia sẻ bạn xem ngay.
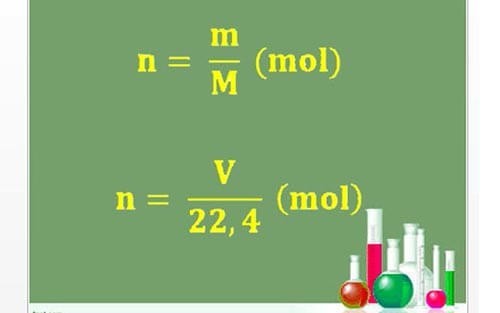
1. Cách tính số mol nguyên tử, phân tử theo khối lượng
n = m/M
Trong đó :
- n là số mol chất (mol).
- M là khối lượng mol (g/mol): Là khối lượng mol của chất đó tính ra gam của N phân tử hoặc nguyên tử chất đó. Khối lượng mol có giá trị bằng phân tử khối hoặc phân tử khối của chất đó như khối lượng mol nguyên tử cacbon – C là 12 g/mol, khối lượng mol của phân tử amoniac – NH3 là 17 g/mol.
Các bạn cần chú ý rằng, khối lượng mol của nguyên tử và phân tử là không giống nhau. Ví dụ, khối lượng mol của phân tử Nito – N2 là 28 g/mol còn khối lượng mol của nguyên tử Nito – N là 14 g/mol - m là khối lượng của chất đó (g).
2. Cách tính số mol của chất khí ở điều kiện tiêu chuẩn (đktc)
n = V/22,4
Trong đó :
- n là số mol chất khí (mol).
- V là thể tích chất khí ở điều kiện tiêu chuẩn (lít).
- 22,4 là hằng số trong điều kiện tiêu chuẩn.
Đối với trường hợp chất khí ở trạng thái tự nhiên, điều kiện khác với điều kiện tiêu chuẩn, bạn không thể sử dụng công thức trên mà phải cần tới những công thức và phép tính phức tạp hơn.
Công thức tính nồng độ mol
CM = n/V
Trong đó :
- CM Nồng độ mol
- n số mol chất tan
- V thể tích dung dịch
Lý giải: Nồng độ mol bằng số mol chất tan chia cho thể tích dung dịch.
Công thức tính nồng độ phần trăm
C% = mct/mdd x 100%
Trong đó:
- C%: Nồng độ phần trăm
- mct: Khối lượng chất tan
- mdd: Khối lượng dung dịch
Mặt khác: mdd = mct + mdm (mdm là khối lượng của dung môi)
Lý giải : Nồng độ phần trăm bằng khối lượng chất tan chia cho khối lượng dung dịch và nhân với một trăm phần trăm.
Bài tập về công thức tính số mol, nồng độ mol và nồng độ phần trăm có đáp án
Bài tập 1: Cho 14,4 lít nước hãy tính nồng độ mol của dung dịch khi hòa tan hết hoàn toàn 31,6g KMnO4 trong đó
Lời giải:
Ta có số mol của KMnO4 là:
nKMnO4 = 31,6/15,8=0,2 (mol)
Nồng độ mol của dung dịch sẽ là : Cm=0,2/31,6=0,0139
Bài tập 2: Tính nồng độ mol của dung dịch khi hòa tan 32 gam NaOH vào trong 400ml nước. Giải thích.
Lời giải :
Đổi: 400ml =0,4 lít
nNaOH = 32/80= 0,4 mol
Áp dụng công thức tính nồng độ mol:
C%= ( CMxM)/(10xD)
Trong đó:
CM=n
V=0,8:0,4= 2M
Tính nồng độ mol của 5 lít dung dịch có chứa 0,5 mol NaCl.
Lời giải:
Nồng độ mol sẽ được tính như sau:
CM = 0,5/5 = 0,1M
Bài tập 3 : Tính nồng độ mol của dung dịch khi hòa tan 15,8g KMnO4 trong 5 lít nước.
Lời giải:
Số mol của KMnO4 là: nKMnO4 = 15,8/158 =0,1 (mol)
Nồng độ mol của dung dịch: CM = 0,1/5 =0,02M
Bài tập 4: Trong 100ml dung dịch có hòa tan 8 gam NaOH. Tính nồng độ mol của dung dịch.
Lời giải :
Ta có V = 100ml = 0,1 lít
nNaOH = 8/40 = 0,2 mol
Áp dụng công thức trên ta có:
CM = n/V =0,2/0,1= 2M
Bài tập 5: Hòa tan hết 20 gam NaCl vào trong 40 gam nước. Hãy tính nồng độ phần trăm của dung dịch này.
Lời giải:
Ta có khối lượng dung dịch là: mdd = mct + mdm = 20 + 40 = 60 gam
Vậy nồng độ phần trăm dung dịch là: C%= x 100% = x 100%= 33,3 %.
Kết luận: Vậy nồng độ dung dịch của NaCl là 33,3%.
Bài tập 6: Hoà tan 10 gam đường vào 40 gam nước. Hãy tính nồng độ phần trăm của dung dịch thu được.
Lời giải:
Ta có khối lượng dung dịch là: mdd = mct + mdm = 10 + 40 = 50 gam
Vậy nồng độ phần trăm dung dịch là: C%= x 100% = x 100%= 20 %.
Kết luận: Vậy nồng độ dung dịch của đường là 20%
Sau khi đọc xong bài viết của chúng tôi có thể giúp các bạn nhớ được công thức tính số mol, nồng độ mol và nồng độ phần trăm để vận dụng vào làm bài tập chính xác nhé